Grafiitti, molekyylikaava: C, molekyylipaino: 12,01, on alkuaineen hiilen muoto, jokainen hiiliatomi on yhdistetty kolmella muulla hiiliatomilla (joka on järjestetty hunajakennoiksi kuusikulmioiksi) muodostaen kovalenttisen molekyylin. Koska jokainen hiiliatomi emittoi elektroneja, jotka voivat liikkua vapaasti, joten grafiitti on johdin.
Grafiitti on yksi pehmeimmistä mineraaleista, ja sen käyttötarkoituksiin kuuluu kynäkynän lyijykynän ja voiteluaineiden valmistus. Hiili on ei-metallinen alkuaine, joka sijaitsee jaksollisen järjestelmän toisen syklin IVA-ryhmässä. Grafiittia muodostuu korkeissa lämpötiloissa.
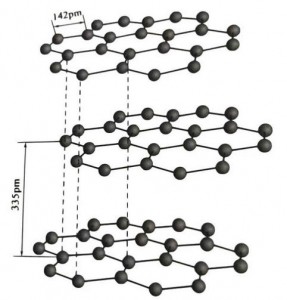
Grafiitti on hiilialkuaineiden kiteinen mineraali, ja sen kiteinen hila on kuusikulmainen kerrosrakenne. Kunkin verkkokerroksen välinen etäisyys on 3,35 A ja hiiliatomien etäisyys samassa verkkokerroksessa on 1,42 A. Se on kuusikulmainen kidejärjestelmä, jossa on täydellinen kerrostettu pilkkoutuminen. Katkaisupinta on pääasiassa molekyylisidoksia, vähemmän houkutteleva molekyyleille, joten sen luonnollinen kelluvuus on erittäin hyvä.
Grafiittikiteissä samassa kerroksessa olevat hiiliatomit muodostavat kovalenttisen sidoksen sp2-hybridisaatiolla, ja jokainen hiiliatomi on kytketty kolmeen muuhun atomiin kolmella kovalenttisella sidoksella. Kuusi hiiliatomia muodostavat samassa tasossa kuuden jatkuvan renkaan, joka ulottuu lamellirakenteeseen, jossa CC-sidoksen sidospituus on 142 pm, mikä on täsmälleen atomikiteen sidoksen pituusalueella, eli samalle kerrokselle , se on atomikide. Samassa tasossa olevilla hiiliatomeilla on yksi p-kiertorata, jotka menevät päällekkäin. Elektronit ovat suhteellisen vapaita, mikä vastaa metallien vapaita elektroneja, joten grafiitti voi johtaa lämpöä ja sähköä, mikä on metallikiteille ominaista. Siten myös luokitellaan metallikiteiksi.
Grafiittikiteen keskikerrosta erottaa 335 pm, ja etäisyys on suuri. Se on yhdistetty van der Waalsin voimaan, eli kerros kuuluu molekyylikiteeseen. Kuitenkin, koska hiiliatomien sitoutuminen samassa tasokerroksessa on erittäin voimakasta ja erittäin vaikea tuhota, on myös grafiitin liukenemispiste erittäin korkea ja sen kemialliset ominaisuudet vakaat.
Koska sen erityinen liimaustapa, ei voida pitää yksikiteinen tai monikiteinen, grafiittia pidetään nykyään yleisesti sekakiteenä.
Postitusaika: 31.7.2023